# SARS-CoV-2, COVID-19, air liur, kit diagnostik
abstrak
cepat dan akurat SARS-CoV-2 pengujian diagnostik penting untuk mengendalikan COVID-19 yang sedang berlangsung pandemi. Standar emas saat ini untuk COVID-19 diagnosis real-time RT-PCR deteksi SARS-CoV-2 dari nasofaring penyeka. sensitivitas rendah, risiko pajanan terhadap petugas kesehatan, dan kekurangan penyeka dan peralatan pelindung diri secara global, bagaimanapun, memerlukan validasi pendekatan diagnostik baru. air liur merupakan kandidat yang menjanjikan untuk SARS-CoV-2 diagnostik karena (1) koleksi minimal invasif dan andal dapat diberikan sendiri dan (2) air liur telah menunjukkan kepekaan yang sebanding terhadap usap nasofaring dalam mendeteksi patogen pernapasan lainnya, termasuk virus korona manusia endemik, dalam penelitian sebelumnya. Untuk memvalidasi penggunaan air liur untuk SARS-CoV-2 deteksi, kami menguji sampel nasofaring dan air liur dari dikonfirmasi COVID-19 pasien dan sampel yang dikumpulkan sendiri dari petugas kesehatan di COVID-19 bangsal. Kapan kami membandingkan SARS-CoV-2 deteksi dari cocok dengan pasien nasofaring
dan sampel air liur, kami menemukan bahwa air liur menghasilkan sensitivitas dan konsistensi deteksi yang lebih besar selama proses infeksi. Selain itu, kami melaporkan lebih sedikit variabilitas dalam sampel mandiri koleksi air liur. diambil bersama, temuan kami menunjukkan bahwa air liur adalah alternatif yang layak dan lebih sensitif untuk usap nasofaring dan bisa aktifkan di rumah dikelola sendiri pengambilan sampel untuk skala besar yang akurat SARS-CoV-2 pengujian.
pengantar
upaya pengendalian SARS-CoV-2, novel coronavirus menyebabkan COVID-19 pandemi, bergantung pada pengujian diagnostik yang akurat dan cepat. Ini tes harus ( 1 ) sensitif terhadap infeksi ringan dan asimtomatik untuk mempromosikan isolasi diri yang efektif dan mengurangi penularan dalam risiko tinggi grup1 ; ( 2 ) konsisten untuk memantau perkembangan penyakit dan bantuan klinis keputusan2 ; dan ( 3 ) terukur untuk menginformasikan kebijakan kesehatan masyarakat lokal dan nasional, seperti kapan langkah-langkah jarak sosial dapat dengan aman santai. Namun, saat ini SARS-CoV-2 strategi pengujian sering gagal untuk memenuhi ini kriteria, sebagian karena dari mereka ketergantungan pada usap nasofaring sebagai jenis sampel yang banyak direkomendasikan untuk real-time RT-PCR.
Meskipun usap nasofaring biasanya digunakan dalam diagnosis virus pernapasan, mereka menunjukkan sensitivitas yang relatif buruk untuk SARS-CoV-2 deteksi pada infeksi dini dan 2–6 tidak konsisten selama pengujian serial . Selain itu, pengambilan usap nasofaring menyebabkan ketidaknyamanan pada pasien karena prosedur invasif, membatasi kepatuhan untuk pengujian berulang, dan menghadirkan risiko yang cukup besar bagi petugas kesehatan, karena dapat menyebabkan pasien bersin atau batuk, mengeluarkan virus partikel7 . Prosedur ini juga tidak kondusif untuk pengujian skala besar, karena ada kekurangan penyeka dan alat pelindung diri untuk perawatan kesehatan pekerja8 , dan koleksi sendiri usap nasofaring sulit dan kurang sensitif terhadap virus deteksi9 . Ini tantangan akan semakin diperburuk sebagai COVID-19 Pandemi meningkat di negara-negara berpenghasilan rendah. mengingat keterbatasan, yang lebih andal dan tidak intensif sumber daya metode pengumpulan sampel, idealnya yang mengakomodasi self-collection di rumah, sangat dibutuhkan. pengambilan sampel saliva adalah alternatif yang menarik untuk usap nasofaring, karena mengumpulkan air liur non-invasif dan mudah dikelola sendiri. analisis kesesuaian nasofaring dan saliva untuk RT-PCR deteksi patogen pernapasan, termasuk dua musiman
virus korona manusia, menunjukkan sensitivitas diagnostik yang sebanding antara dua sampel 10,11dari COVID-19 pasien dan ( 2 ) sampel air liur yang dikumpulkan sendiri memiliki sebanding. temuan awal menunjukkan bahwa ( 1 ) SARS-CoV-2 dapat dideteksi dari air liur 12 tipemSARS-CoV-2 sensitivitas deteksi terhadap usap nasofaring yang dikumpulkan oleh perawatan kesehatan 13pekerja dari ringan dan subklinis COVID-19 kasus . Namun secara kritis, tidak ada evaluasi yang ketat terhadap sensitivitas SARS-CoV-2 deteksi dalam saliva sehubungan dengan usap nasofaring telah dilakukan dari rawat inap selama perjalanan COVID-19 infeksi.
dalam studi ini, kami mengevaluasi SARS-CoV-2 deteksi pada usap nasofaring berpasangan dan sampel air liur yang dikumpulkan dari COVID-19 pasien rawat inap dan petugas perawatan kesehatan tanpa gejala di sedang hingga tinggi risiko COVID-19 eksposur. Kami hasil menunjukkan bahwa menggunakan saliva untuk SARS-CoV-2 deteksi lebih sensitif dan konsisten daripada menggunakan nasofaring penyeka. Secara keseluruhan, kami menunjukkan bahwa air liur harus dianggap sebagai jenis sampel yang dapat diandalkan untuk mengurangi COVID-19 pengujian tuntutan.
hasil
lebih tinggi SARS-CoV-2 titer terdeteksi dari air liur dari usap nasofaring dari pasien rawat inap
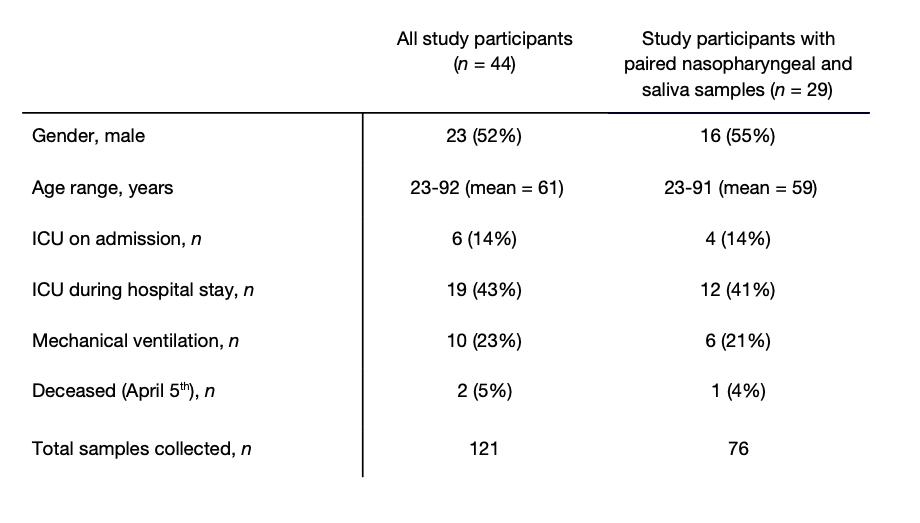
Untuk menentukan apakah air liur bekerja sebaik AS rekomendasi cdc tentang penggunaan usap nasofaring untuk SARS-CoV-2 diagnosa, kami mengumpulkan sampel klinis dari 44 COVID-19 peserta studi rawat inap ( Tabel 1 ). Ini kohort mewakili rentang COVID-19 pasien dengan penyakit parah, dengan 19 (43%) membutuhkan perawatan intensif, 10 (23%) membutuhkan ventilasi mekanis, dan 2 (5%) meninggal per 5 April 2020. menggunakan a.s. cdc SARS-CoV-2 RT-PCR assay, kami menguji 121 air liur yang dikumpulkan sendiri atau perawatan kesehatan yang dikelola oleh pekerja usap nasofaring dari ini kelompok. Kami menemukan kesesuaian yang kuat antara AS cdc “N1” dan “N2” pemeriksaan primer set ( data diperpanjang Gambar. 1), dan dengan demikian menghitung titer virus (virus salinan / mL) hanya menggunakan "N1" set. Dari semua sampel positif diuji ( n = 46 nasopharyngeal, 37 saliva), kami menemukan bahwa geometri rata-rata titer virus dari air liur sekitar 5⨉ lebih tinggi dari usap nasofaring ( p < 0,05, Mann-Whitney Uji; Gambar. 1a ). Kapan membatasi analisis kami hanya dengan pasien yang cocok sampel nasofaring dan saliva ( n = 38 untuk setiap jenis sampel), kami menemukan bahwa SARS-CoV-2 titer dari saliva secara signifikan lebih tinggi daripada usap nasofaring ( p = 0,0001, Wilcoxon Uji; Gambar. 1b ). Selain itu, kami mendeteksi SARS-CoV-2 dari air liur tapi tidak usap nasofaring dari delapan sampel yang cocok (21%), sementara kami hanya mendeteksi SARS-CoV-2 dari usap nasofaring dan bukan air liur dari tiga sampel yang cocok (8%; Gambar. 1c ). Secara keseluruhan, kami menemukan lebih tinggi SARS-CoV-2 titer dari air liur dari usap nasofaring dari rumah sakit rawat inap.
tabel 1. COVID-19 karakteristik kelompok rawat inap
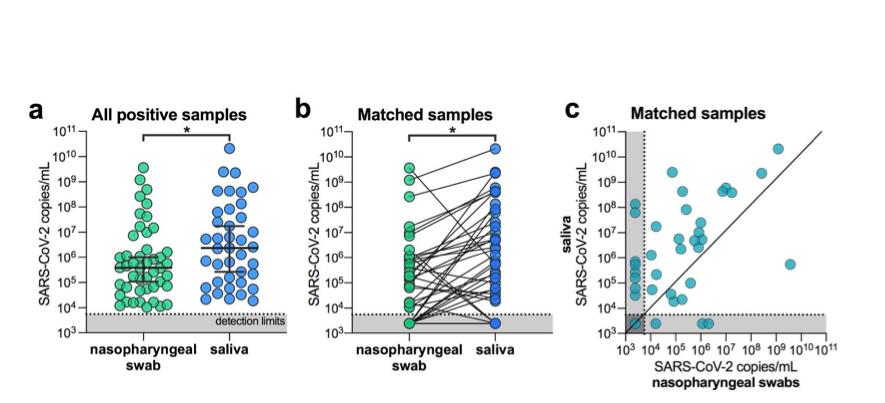
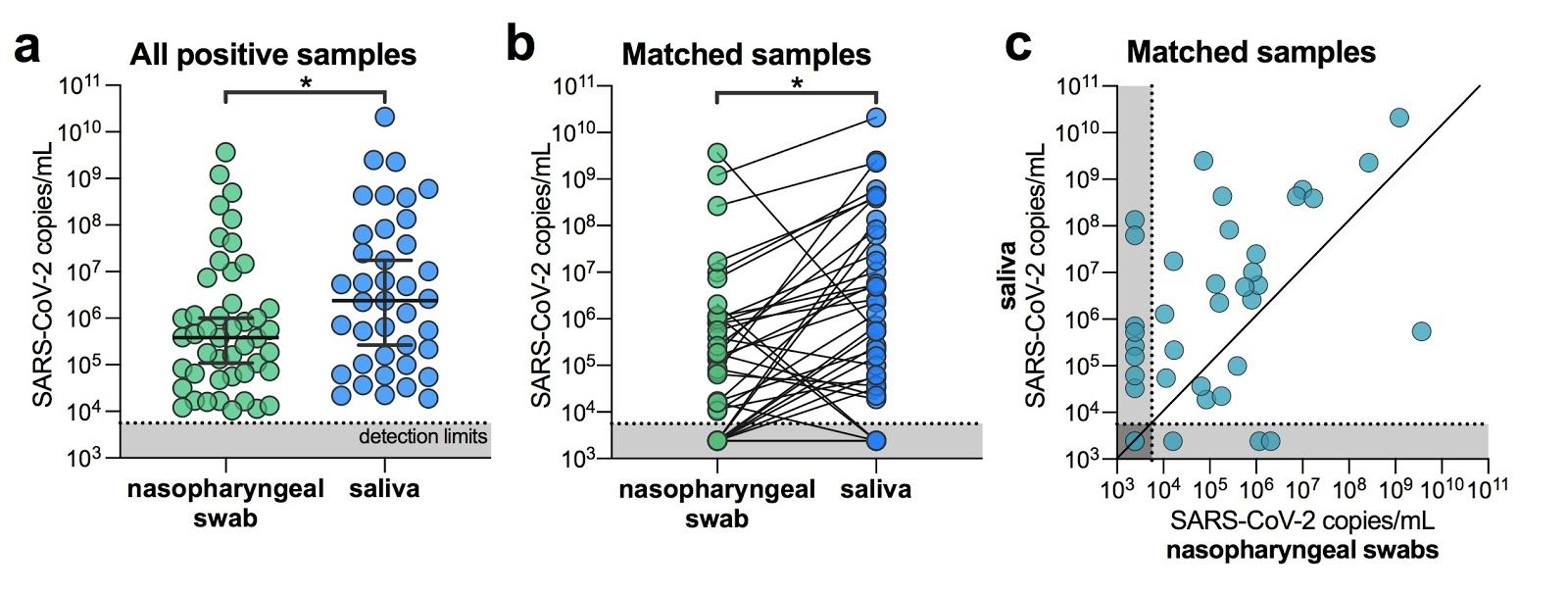
gambar 1. SARS-CoV-2 titer lebih tinggi di saliva daripada usap nasofaring dari rumah sakit rawat inap. ( Sebuah ) semua usapan nasofaring positif ( n = 46) dan sampel air liur ( n = 39) dibandingkan dengan Mann-Whitney tes ( p < 0,05). batang mewakili median dan 95% CI. Kami batas deteksi uji untuk SARS-CoV-2 menggunakan us cdc “N1” pengujian berada pada ambang siklus 38, yang sesuai dengan 5.610 virus salinan / mL sampel (ditampilkan sebagai garis putus-putus dan abu-abu area). ( b ) pasien cocok sampel ( n = 38), diwakili oleh garis penghubung, dibandingkan dengan Wilcoxon uji uji ( p < 0,05). ( c ) pasien cocok sampel ( n = 38) juga diwakili pada sebaran plot. semua data yang digunakan untuk menghasilkan gambar ini, termasuk ambang siklus mentah, dapat ditemukan di data pelengkap 1 . data diperpanjang Gambar. 1menunjukkan korelasi antara kami cdc assay "N1" dan “N2” Hasil.
kurang temporal SARS-CoV-2 variabilitas saat menguji air liur dari pasien rawat inap
sebagai temporal SARS-CoV-2 pengujian diagnostik dari usap nasofaring dilaporkan 2,3variabel, kami menguji sampel nasofaring dan saliva longitudinal dari pasien rawat inap untuk menentukan jenis sampel yang memberikan hasil yang lebih konsisten. Dari Dari 22 peserta dengan beberapa usapan nasofaring dan 12 peserta dengan beberapa sampel air liur, kami menemukan bahwa SARS-CoV-2 titer umumnya menurun pada kedua jenis sampel setelah tanggal onset gejala yang dilaporkan ( Gambar. 2a ). Kami Hasil usap nasofaring konsisten dengan 2,3laporan variabel sebelumnya SARS-CoV-2 titer dan hasil : kami menemukan 5 contoh dimana a peserta usap nasofaring negatif untuk SARS-CoV-2 diikuti dengan hasil positif selama koleksi berikutnya (5 / 33 berulang, 33%; Gambar. 2b ) . dalam koleksi saliva longitudinal dari 12 pasien, bagaimanapun, tidak ada contoh di mana sampel diuji negatif dan kemudian diikuti dengan hasil positif karena hasil tes negatif sebenarnya penting bagi dokter untuk melacak peningkatan pasien dan untuk keputusan tentang pembuangan, data kami menunjukkan bahwa air liur adalah jenis sampel yang lebih konsisten daripada usap nasofaring untuk memantau perubahan temporal pada SARS-CoV-2 titer.
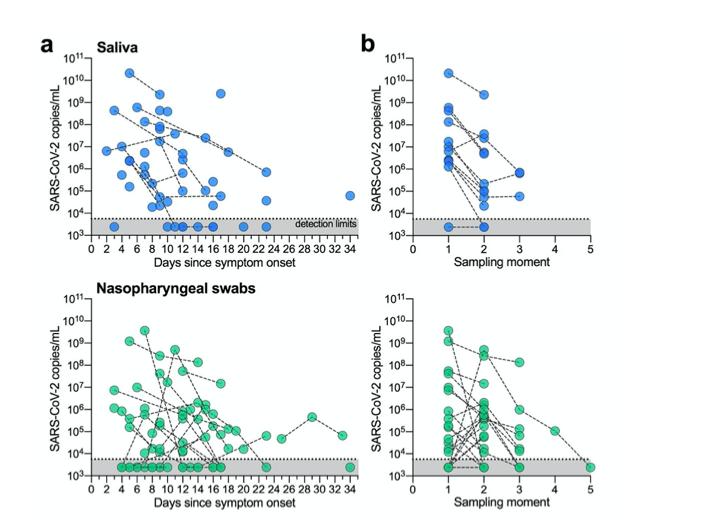
gambar 2: SARS-CoV-2 Deteksi kurang bervariasi antara pengumpulan sampel berulang dengan saliva. (a) longitudinal SARS-CoV-2 titer dari saliva atau usap nasofaring ditampilkan sebagai hari sejak gejala onset. setiap lingkaran mewakili sampel terpisah, yang terhubung ke sampel tambahan dari pasien yang sama dengan garis putus-putus. Kami batas deteksi uji untuk SARS-CoV-2 menggunakan us cdc “N1” pengujian berada pada ambang siklus 38, yang sesuai dengan 5.610 virus salinan / mL sampel (ditampilkan sebagai garis putus-putus dan abu-abu area). ( b ) Data juga ditampilkan oleh momen pengambilan sampel (sekuensial pengumpulan waktu) untuk menyoroti perbedaan titer virus di antara kumpulan poin. semua data yang digunakan untuk menghasilkan gambar ini, termasuk ambang siklus mentah, dapat ditemukan di data pelengkap 1 .
lebih konsisten pengambilan sampel sendiri dari petugas kesehatan menggunakan air liur
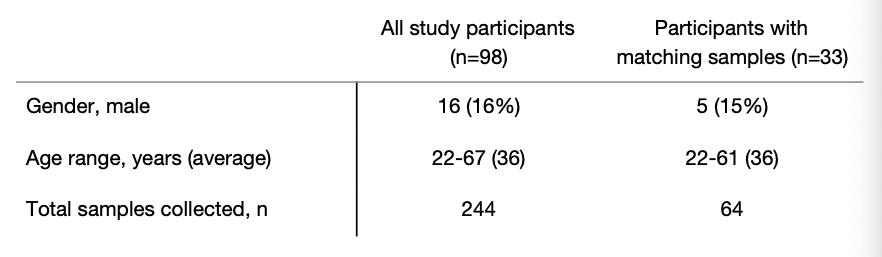
memvalidasi saliva untuk deteksi subklinis SARS-CoV-2 infeksi bisa membuktikan transformatif untuk diagnosis pasien jarak jauh dan petugas kesehatan pengawasan. Untuk menyelidiki ini, kami mendaftarkan 98 petugas perawatan kesehatan tanpa gejala ke dalam penelitian kami dan mengumpulkan air liur dan / atau rata-rata usap nasofaring setiap 2.9 hari (range = 1-8 hari, Meja 2 ). Untuk tanggal, kami telah mendeteksi SARS-CoV-2 dalam air liur dari dua petugas kesehatan yang negatif dengan usapan nasofaring menggunakan us cdc “N1” dan “N2” tes dan tidak melaporkan gejala apapun. Air liur dari salah satu dari ini individu kembali dites positif di samping usap nasofaring negatif yang cocok atas ulangi pengujian 2 hari nanti. titer virus dari perawatan kesehatan tanpa gejala pekerja air liur lebih rendah dari apa kami biasanya mendeteksi dari pasien rawat inap simtomatik ( Gambar. 3a ), yang kemungkinan mendukung kurangnya gejala.
Kami data terbatas mendukung bahwa air liur mungkin lebih sensitif untuk mendeteksi asimtomatik atau pra-gejala infeksi; Namun, ukuran sampel yang lebih besar diperlukan untuk konfirmasi. karena inkonsistensi pengambilan sampel usap nasofaring dapat menjadi salah satu masalah potensial untuk negatif palsu ( Gambar. 2), memantau pengendalian internal untuk pengumpulan sampel yang tepat, human rnase P, dapat memberikan evaluasi alternatif teknik. sementara deteksi p rnase manusia lebih baik dari air liur pada pasien rawat inap dan petugas kesehatan ( Gambar. 3b ) , ini saja mungkin tidak menunjukkan deteksi virus yang lebih baik. lebih penting lagi, kami menemukan bahwa deteksi p rnase manusia lebih bervariasi dari usap nasofaring dikumpulkan dari pasien rawat inap ( p = 0,0001, uji f untuk varians) dan dikumpulkan sendiri dari petugas kesehatan ( p = 0,0002; Gambar. 3b ). Kami Hasil menunjukkan bahwa air liur mungkin juga merupakan alternatif yang tepat, dan mungkin lebih sensitif, dari usap nasofaring untuk skrining asimtomatik atau pra-gejala SARS-CoV-2 Infeksi.
tabel 2. kohort petugas kesehatan
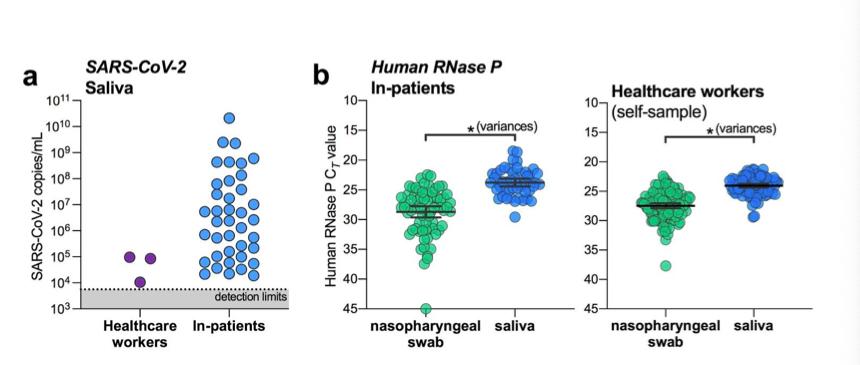
gambar 3. air liur merupakan alternatif untuk SARS-CoV-2 pemutaran dari petugas kesehatan dan kasus asimtomatik. ( Sebuah ) SARS-CoV-2 titer diukur dari air liur petugas kesehatan dan pasien rawat inap. Kami batas deteksi uji untuk SARS-CoV-2 menggunakan us cdc “N1” pengujian berada pada ambang siklus 38, yang sesuai dengan 5.610 virus salinan / mL sampel (ditampilkan sebagai garis putus-putus dan abu-abu area). ( b ) RT-PCR ambang batas siklus (Ct) nilai untuk rnase P manusia, dan pengendalian internal untuk pengumpulan sampel, dari baik pasien rawat inap (kiri panel) atau petugas kesehatan (kanan panel) dibandingkan dengan varians menggunakan uji f ( p = 0,0001 untuk pasien rawat inap; p = 0,0002 untuk kesehatan pekerja). semua data yang digunakan untuk menghasilkan gambar ini, termasuk ambang siklus mentah, dapat ditemukan di data pelengkap 1 .
diskusi
Kami studi menunjukkan bahwa air liur adalah alternatif yang layak dan lebih disukai daripada usap nasofaring untuk SARS-CoV-2 Deteksi. Kami menemukan bahwa sensitivitas SARS-CoV-2 deteksi dari air liur sebanding, jika tidak lebih baik dari usap nasofaring pada awal rawat inap dan lebih konsisten selama diperpanjang rawat inap dan pemulihan. Apalagi, deteksi SARS-CoV-2 dari air liur dua petugas perawatan kesehatan tanpa gejala meskipun hasil usap nasofaring negatif menunjukkan bahwa air liur juga dapat menjadi alternatif yang layak untuk mengidentifikasi infeksi ringan atau subklinis. Dengan validasi lebih lanjut, penerapan luas pengambilan sampel saliva bisa menjadi transformatif untuk kesehatan masyarakat upaya: air liur pengumpulan sendiri meniadakan kebutuhan untuk perawatan kesehatan langsung pekerja-pasien interaksi, sumber 14–16 beberapa hambatan pengujian utama dan risiko infeksi nosokomial secara keseluruhan, dan mengurangi permintaan pasokan pada penyeka dan peralatan pelindung diri.
AsSARS-CoV-2vialloadsdifferbetweenmildandseverecases , batasan penelitian kami adalah fokus utama pada COVID-19 pasien rawat inap, banyak dengan penyakit parah. sementara lebih banyak data diperlukan untuk membandingkan secara lebih ketat keefektifan air liur di rumah sakit dengan awal infeksi, temuan dari dua studi terbaru mendukung potensinya 13,18 mendeteksi SARS-CoV-2 dari baik individu tanpa gejala dan pasien rawat jalan . sebagai 12 virus menular telah terdeteksi dari air liur COVID-19 pasien, memastikan hubungan antara salinan genom virus dan partikel virus infeksius dalam air liur 19 pra-gejala individu akan memainkan peran kunci dalam memahami dinamika 1,20asimtomatik transmisi.
berasal dari hasil yang menjanjikan untuk SARS-CoV-2 Deteksi asimtomatik 13
individu, asaliva deteksi SARS-CoV-2 telah memperoleh persetujuan melalui
kami. otorisasi penggunaan darurat administrasi makanan dan obat . Untuk memenuhi permintaan pengujian yang terus meningkat, namun, temuan kami mendukung kebutuhan untuk segera validasi dan implementasi air liur untuk SARS-CoV-2 diagnostik di klinis bersertifikat laboratorium.
metode
etika
semua peserta studi terdaftar dan diambil sampelnya sesuai dengan universitas yale disetujui HIC protokol # 2000027690. Demografi, data klinis dan sampel hanya dikumpulkan setelah partisipan penelitian mengakui bahwa mereka telah memahami protokol penelitian dan menandatangani informed consent. semua informasi dan sampel peserta dikumpulkan dalam kaitannya dengan studi pengidentifikasi.
pendaftaran peserta
pasien rawat inap
pasien dirawat di rumah sakit surga baru yale (a 1541 tempat tidur pusat medis perawatan tersier di New Haven, CT, AS), yang dites positif untuk SARS-CoV-2 oleh nasopharyngeal dan / atau usap oropharyngeal (CDC disetujui uji) diundang untuk mendaftar dalam penelitian studi. kriteria eksklusi adalah usia di bawah 18 tahun, non-Inggris berbicara dan bukti klinis, radiologis atau laboratorium untuk tidak menular penyebab demam atau gejala pernapasan atau dikonfirmasi secara mikrobiologis sumber infeksius (misalnya gastrointestinal, kemih, kardiovaskular) selain saluran pernapasan untuk gejala dan tidak ada kecurigaan untuk COVID-19 infeksi.
petugas kesehatan
petugas perawatan kesehatan tanpa gejala (misalnya, tanpa demam atau gejala pernapasan) dengan pajanan pada pasien dengan COVID-19 diundang untuk mendaftar di studi. partisipasi studi memungkinkan pengawasan aktif untuk memastikan deteksi dini setelah pajanan dan untuk lebih melindungi petugas kesehatan lain dan pasien.
pengumpulan sampel
pasien rawat inap
sampel nasofaring dan saliva diambil setiap tiga hari selama mereka klinis Tentu saja. Sampel nasofaring diambil oleh perawat terdaftar menggunakan bd universal viral transport (UVT) sistem. Fleksibel, tip mini usap melewati pasien lubang hidung sampai nasofaring posterior tercapai, dibiarkan di tempatnya selama beberapa detik untuk menyerap sekresi kemudian perlahan dikeluarkan sambil berputar. Usap ditempatkan di media transpor virus steril (total volume 3 mL) dan disegel dengan aman. Sampel saliva diambil sendiri oleh pasien. Setelah bangun, pasien diminta untuk menghindari makanan, air dan menyikat gigi sampai sampel dikumpulkan. pasien diminta untuk berulang kali meludah ke cangkir urin steril sampai kira-kira sepertiga penuh cairan (tidak termasuk gelembung), sebelum menutupnya dengan aman. semua sampel disimpan pada suhu kamar dan diangkut ke laboratorium penelitian di sekolah kesehatan masyarakat yale dalam waktu 5 jam setelah pengambilan sampel.
petugas kesehatan
petugas kesehatan diminta untuk mengumpulkan dikelola sendiri usap nasofaring dan sampel air liur setiap tiga hari selama 2 minggu. sampel disimpan pada + 4 ° C sampai sedang diangkut ke penelitian lab.
SARS-CoV-2 deteksi
setibanya di lab penelitian, total nukleat asam diekstraksi dari 300 μl media transportasi virus dari usap nasofaring atau 300 μl seluruh air liur menggunakan MagMAX Virus / Patogen Nuklir kit isolasi asam (ThermoFisher Ilmiah) mengikuti pabrikan protokol dan dielusi menjadi 75 μl elusi penyangga. Untuk SARS-CoV-2 rna 21,22 deteksi, 5 μl template rna diuji seperti yang dijelaskan sebelumnya, menggunakan us cdc real-time RT-PCR primer / probe ditetapkan untuk 2019-nCoV_N1 dan 2019-nCoV_N2 dan rnase manusia p (RP) sebagai ekstraksi kontrol. sampel diklasifikasikan sebagai positif untuk SARS-CoV-2 ketika keduanya N1 dan N2 pemeriksaan primer set terdeteksi <38 c . salinan virus t dikuantifikasi menggunakan 10 kali lipat kurva standar pengenceran transkrip rna yang kita sebelumnya 21dihasilkan . sebagai hasil dari N1 dan N2 sebanding ( data diperpanjang Gambar. 1), semua salinan virus ditampilkan sebagaimana dihitung menggunakan N1 pemeriksaan primer set.
Analisis statistik
analisis statistik dilakukan di GraphPad prisma 8.0.0 seperti yang dijelaskan dalam Hasil.
ucapan terima kasih
Kami berterima kasih kepada peserta studi atas mereka waktu dan komitmen untuk studi. Kami terima kasih kepada semua anggota tim klinis di Yale-New surga rumah sakit untuk mereka dedikasi dan kerja keras yang memungkinkan studi ini Kami juga terima kasih S. taylor dan P. jack untuk diskusi teknis.
pendanaan
Studi ini sebagian didanai oleh yale institute for global Health. Penulis terkait memiliki akses penuh ke semua data dalam penelitian dan memiliki tanggung jawab akhir atas keputusan untuk mengirimkan publikasi.
data diperpanjang
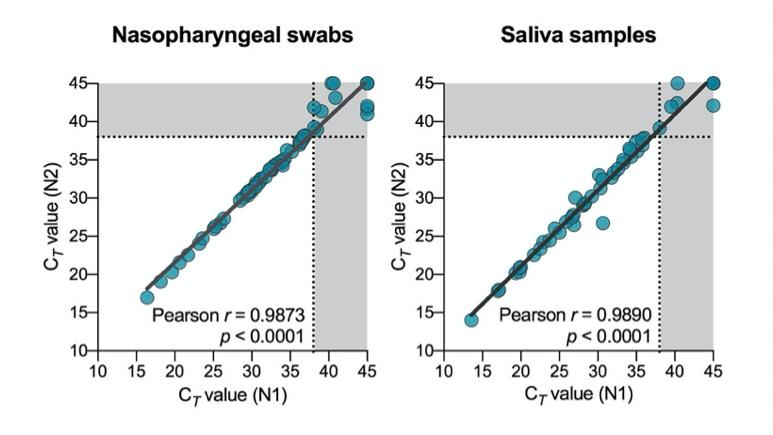
data diperpanjang Gambar. 1. kesesuaian antara SARS-CoV-2 deteksi menggunakan kami cdc “N1” dan “N2” primer dan probe set. ct = RT-PCR siklus ambang batas. garis putus-putus dan area abu-abu menunjukkan batas deteksi.
referensi
1. Kimball, A. et al. asimtomatik dan tanpa gejala SARS-CoV-2 infeksi pada penghuni fasilitas perawatan terampil perawatan jangka panjang - king County, Washington, Maret 2020. MMWR Morb. Manusia. Wkly. Rep. 69, 377–381 (2020).
2. Wölfel, R. et al. penilaian virologi pasien rawat inap dengan COVID-2019. alam (2020) doi: 10.1038 / s41586-020-2196-x.
3. Zou, L. et al. SARS-CoV-2 viral load dalam spesimen saluran pernapasan atas dari pasien yang terinfeksi N. Engl. J. Med. 382 , 1177–1179 (2020).
4. Zhao, J. et al. tanggapan antibodi terhadap SARS-CoV-2 pada pasien novel coronavirus penyakit 2019. Clin. Infeksi. Dis. (2020) doi: 10.1093 / cid / ciaa344.
5. Xie, X. et al. chest ct untuk tipikal 2019-nCoV Pneumonia: hubungan ke negatif RT-PCR Pengujian. radiologi 200343 (2020).
6. Wang, W. et al. deteksi SARS-CoV-2 dalam berbagai jenis klinis Spesimen. JAMA (2020) doi: 10.1001 / jama.2020.3786.
7. Kepada, K. K.-W. et al. profil temporal viral load dalam sampel saliva orofaring posterior dan respon antibodi serum selama infeksi oleh SARS-CoV-2: sebuah kelompok observasi studi. lancet Infeksi. Dis. (2020) doi: 10.1016 / S1473-3099 (20) 30196-1.
8. CDC. rekomendasi pencegahan dan pengendalian infeksi sementara untuk pasien yang dicurigai atau dikonfirmasi Coronavirus penyakit 2019 (COVID-19) dalam perawatan kesehatan Pengaturan. Pusat Pengendalian dan Pencegahan Penyakit https: / / www.cdc.gov / coronavirus / 2019-ncov / hcp / rekomendasi-pengendalian-infeksi.h tml? CDC_AA_refVal = https% 3A% 2F% 2Fwww.cdc.gov% 2Fcoronavirus% 2F2019-ncov % 2Finfection-control% 2Fcontrol-recommend.html (2020).
9. Dhiman, N. et al. efektivitas dikumpulkan pasien penyeka untuk influenza pengujian. mayo Klinik Proc. 87, 548–554 (2012).
10. Kim, Y.-G. et al. perbandingan antara air liur dan spesimen usap nasofaring untuk mendeteksi virus pernapasan dengan multipleks terbalik Transkripsi-PCR. J. Clin. Mikrobiol. 55, 226–233 (2017).
11. Wyllie, A. L. et al. surveilans molekuler pembawa nasofaring dari streptococcus pneumoniae pada anak-anak yang divaksinasi dengan polisakarida pneumokokus terkonjugasi vaksin. Sci. Rep. 6, 23809 (2016).
12. Kepada, K. K.-W. et al. deteksi konsisten dari 2019 novel Coronavirus di Air liur. Clin. Infeksi. Dis. (2020) doi: 10.1093 / cid / ciaa149.
13. Kojima, N. et al. cairan oral yang dikumpulkan sendiri dan usap hidung menunjukkan sensitivitas yang sebanding dengan swab nasofaring yang dikumpulkan oleh klinisi untuk Covid-19 Deteksi. medRxiv 2020.04.11.20062372 (2020).
14. Tran, K., Cimon, K., Severn, M., Pessoa-Silva, C. L. & Conly, J. prosedur yang menimbulkan aerosol dan risiko penularan infeksi saluran pernapasan akut ke layanan kesehatan pekerja: sistematis tinjauan. plos one 7, e35797 (2012).
15. Judson, S. D. & Munster, V. J. transmisi nosokomial dari virus yang muncul melalui Pembangkit Aerosol medis Prosedur. virus 11, (2019).
16. Wang, D. et al. karakteristik klinis dari 138 pasien rawat inap Dengan 2019 novel Terinfeksi Coronavirus pneumonia di Wuhan, China. JAMA (2020) doi: 10.1001 / jama.2020.1585.
17. Liu, Y. et al. dinamika virus dalam kasus ringan dan berat COVID-19. lancet Infeksi. Dis. (2020) doi: 10.1016 / S1473-3099 (20) 30232-2.
18. kami. makanan & obat Administrasi. otorisasi penggunaan darurat yang dipercepat (EUA) ringkasan SARS-CoV-2 assay (Rutgers genomik klinis Laboratorium). https: / / www.fda.gov / media / 136875 / unduh.
19. Lauer, S. A. et al. Masa inkubasi Coronavirus penyakit 2019 (COVID-19) Dari dilaporkan secara publik dikonfirmasi Kasus: estimasi dan Aplikasi. Ann. Magang. Med.
Sumber: https: / / www.medrxiv.org / konten / 10.1101 / 2020.04.16.20067835v1.full.pdf
AnneL.Wyllie1 *, JohnFournier2, ArnauCasanovas-Massana1, MelissaCampbell2, MariaTokuyama3, Pavithra Vijayakumar4 , Bertie Geng4 , M. catherine Muenker1 , adam J. Moore1 , Chantal B.F. Vogels1 , mary E. Petrone1 , Isabel M. Ott5, Peiwen Lu3 , Arvind Venkataraman3 , Alice Lu-Culligan3 , jonathan Klein3 , rebecca Earnest1 , Michael Simonov6 , Rupak Datta2 , Ryan Handoko2 , Nida Naushad2 , Lorenzo R. Sewanan2 , jordan Valdez2 , Elizabeth B. Putih1 , sarah Lapidus1 , Chaney C. Kalinich1 , Xiaodong Jiang3 , daniel J. Kim3 , Eriko Kudo3 , melissa Linehan3 , Tianyang Mao3 , Miyu Moriyama3 , ji Eun Oh3 , Annsea Park3 , Julio Silva3 , Eric Lagu3 , Takehiro Takahashi3 , Manabu Taura3 , Orr-El Weizman3 , patrick Wong3 , Yexin Yang3 , santos Bermejo7 , Camila Odio8 , Saad B. Omer1,2,9,10, charles S. Dela Cruz7 , ShelliFarhadian2, RichardA.Martinello2,7,11, AkikoIwasaki3,12, NathanD.Grubaugh1 # *, AlbertI.Ko1 # *
1 departemen epidemiologi penyakit mikroba, yale school of public health, new Haven, ct 06510, usa 2 departemen kedokteran, bagian penyakit menular, yale school of medicine, new Haven, CT, 06510, usa
3 departemen Imunobiologi, Fakultas Kedokteran Yale, New Haven, CT, 06510, USA
4 departemen Kebidanan, Ginekologi, dan Ilmu Reproduksi, Fakultas Kedokteran Yale, New Haven, CT, 06510, AS
5 departemen ekologi dan biologi evolusioner, yale University, new Haven, ct 06520, USA
6 Program Penelitian Translasional Terapan, Fakultas Kedokteran Yale, New Haven, CT, 06510, USA
7 departemen penyakit dalam, bagian paru-paru, perawatan kritis, dan pengobatan tidur, yale School of Medicine, new Haven, CT, 06510, USA
8 departemen kedokteran, grup medis timur laut, Yale-New haven Health, New Haven, ct 06510, AS
9 yale institute of global Health, New Haven, ct 06510, AS
Sekolah Perawat 10 yale, New Haven, ct 06510, AS
11 departemen Pencegahan infeksi, Yale-New surga Kesehatan, Haven baru, ct 06520
12 Howard Hughes Medical Institute, New Haven, CT 06510, AS
# penulis senior bersama
* Korespondensi: anne.wyllie@yale.edu (ALW); nathan.grubaugh@yale.edu (NDG); albert.ko@yale.edu (AIK)